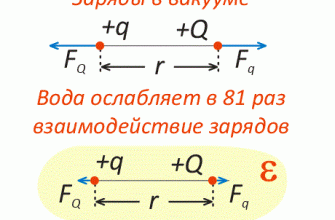
Работа аккумулятора при заряде
 В широком смысле слова в технике под термином «Аккумулятор» понимается устройство, которое позволяет при одних условиях эксплуатации накапливать определенный вид энергии, а при других — расходовать ее для нужд человека.
В широком смысле слова в технике под термином «Аккумулятор» понимается устройство, которое позволяет при одних условиях эксплуатации накапливать определенный вид энергии, а при других — расходовать ее для нужд человека.
Их применяют там, где необходимо собрать энергию за определенное время, а затем использовать ее для совершения больших трудоемких процессов. Например, гидравлические аккумуляторы, используемые в шлюзах, позволяют поднимать корабли на новый уровень русла реки.
Электрические аккумуляторы работают с электроэнергией по этому же принципу: вначале накапливают (аккумулируют) электричество от внешнего источника заряда, а затем отдают его подключенным потребителям для совершения работы. По своей природе они относятся к химическим источникам тока, способным совершать много раз периодические циклы разряда и заряда.
Во время работы постоянно происходят химические реакции между компонентами электродных пластин с заполняющим их веществом — электролитом.
Принципиальную схему устройства аккумулятора можно представить рисунком упрощенного вида, когда в корпус сосуда вставлены две пластины из разнородных металлов с выводами для обеспечения электрических контактов. Между пластинами залит электролит.
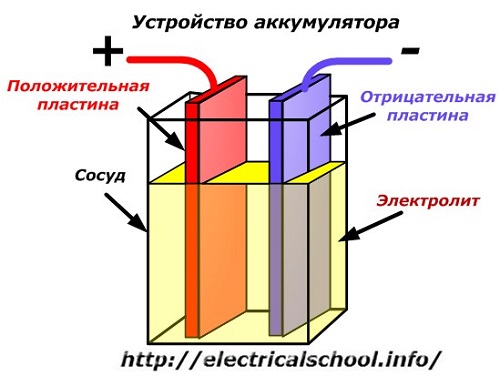
Работа аккумулятора при разряде
Когда к электродам подключена нагрузка, например, лампочка, то создается замкнутая электрическая цепь, через которую протекает ток разряда. Он формируется движением электронов в металлических частях и анионов с катионами в электролите.
Этот процесс условно показан на схеме с никель-кадмиевой конструкцией электродов.
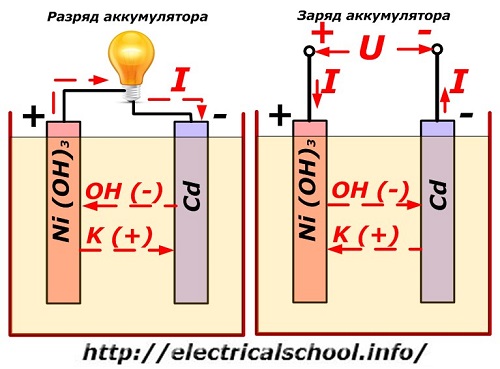
Здесь в качестве материала положительного электрода используют окислы никеля с добавками графита, которые повышают электрическую проводимость. Металлом отрицательного электрода работает губчатый кадмий.
Во время разряда частицы активного кислорода из окислов никеля выделяются в электролит и направляются на отрицательные пластины, где окисляют кадмий.
Работа аккумулятора при заряде
При отключенной нагрузке на клеммы пластин подается постоянное (в определенных ситуациях пульсирующее) напряжение большей величины, чем у заряжаемого аккумулятора с той же полярностью, когда плюсовые и минусовые клеммы источника и потребителя совпадают.
Зарядное устройство всегда обладает большей мощностью, которая «подавляет» оставшуюся в аккумуляторе энергию и создает электрический ток с направлением, противоположным разряду. В результате внутренние химические процессы между электродами и электролитом изменяются. Например, на банке с никель кадмиевыми пластинами положительный электрод обогащается кислородом, а отрицательный — восстанавливается до состояния чистого кадмия.
При разряде и заряде аккумулятора происходит изменение химического состава материала пластин (электродов), а электролита не меняется.
Способы соединения аккумуляторов
Величина тока разряда, которую может выдержать одна банка, зависит от многих факторов, но в первую очередь от конструкции, примененных материалов и их габаритов. Чем значительнее площадь пластин у электродов, тем больший ток они могут выдерживать.
Этот принцип используется для параллельного подключения однотипных банок у аккумуляторов при необходимости увеличения тока на нагрузку. Но для заряда такой конструкции потребуется поднимать мощность источника. Этот способ используется редко для готовых конструкций, ведь сейчас намного проще сразу приобрести необходимый аккумулятор. Но им пользуются производители кислотных АКБ, соединяя различные пластины в единые блоки.
В зависимости от применяемых материалов, между двумя электродными пластинами распространенных в быту аккумуляторов может быть выработано напряжение 1,2/1,5 или 2,0 вольта. (На самом деле этот диапазон значительно шире.) Для многих электрических приборов его явно недостаточно. Поэтому однотипные аккумуляторы подключают последовательно, причем это часто делают в едином корпусе.
Примером подобной конструкции служит широко распространенная автомобильная разработка на основе серной кислоты и свинцовых пластин-электродов.
Обычно в народе, особенно среди водителей транспорта, принято называть аккумулятором любое устройство, независимо от количества его составных элементов — банок. Однако, это не совсем правильно. Собранная из нескольких последовательно подключенных банок конструкция является уже батареей, за которой закрепилось сокращенное название «АКБ» . Ее внутреннее устройство показано на рисунке.
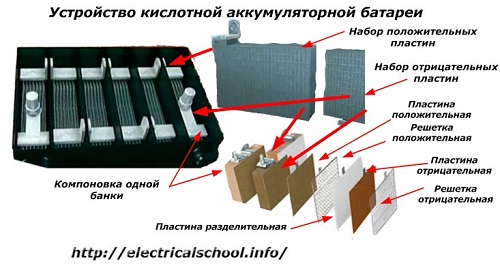
Любая из банок состоит из двух блоков с набором пластин для положительного и отрицательного электродов. Блоки входят друг в друга без металлического контакта с возможностью надежной гальванической связи через электролит.
При этом контактные пластины имеют дополнительную решетку и отдалены между собой разделительной пластиной — сепаратором.
Соединение пластин в блоки увеличивает их рабочую площадь, снижает общее удельное сопротивление всей конструкции, позволяет повышать мощность подключаемой нагрузки.
С внешней стороны корпуса такая АКБ имеет элементы, показанные на рисунке ниже.
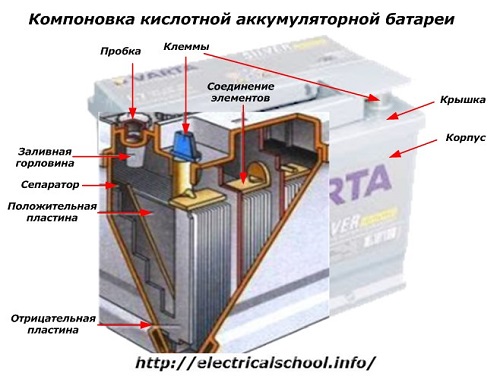
Из него видно, что прочный пластмассовый корпус закрыт герметично крышкой и сверху оборудован двумя клеммами (обычно конусной формы) для подключения к электрической схеме автомобиля. На их выводах выбита маркировка полярности: «+» и «-». Как правило, для блокировки ошибок при подключении диаметр положительной клеммы немного больше, чем у отрицательной.
У обслуживаемых аккумуляторных батарей сверху каждой банки размещена заливная горловина для контроля уровня электролита или доливки дистиллированной воды при эксплуатации. В нее вворачиваются пробка, которая предохраняет внутренние полости банки от попадания загрязнений и одновременно не дает выливаться электролиту при наклонах АКБ.
Поскольку при мощном заряде возможно бурное выделение газов из электролита (а этот процесс возможен при интенсивной езде), то в пробках делаются отверстия для предотвращения повышения давления внутри банки. Через них выходят кислород и водород, а также пары электролита. Подобные ситуации, связанные с чрезмерными токами заряда, желательно избегать.
На этом же рисунке показано соединение элементов между банками и расположение пластин-электродов.
Стартерные автомобильные АКБ (свинцово-кислотные) работают по принципу двойной сульфатации. На них во время разряда/заряда происходит электрохимический процесс, сопровождающийся изменением химического состава активной массы электродов с выделением/поглощением в электролит (серную кислоту) воды.
Этим объясняется повышение удельной плотности электролита при заряде и снижение при разряде батареи. Другими словами, величина плотности позволяет оценивать электрическое состояние АКБ. Для ее замера используют специальный прибор — автомобильный ареометр.
Входящая в состав электролита кислотных батарей дистиллированная вода при отрицательной температуре переходит в твердое состояние — лед. Поэтому, чтобы автомобильные аккумуляторы не замерзали в холодное время, необходимо применять специальные меры, предусмотренные правилами эксплуатации.
Какие существуют типы аккумуляторов
Современное производство для различных целей выпускает более трех десятков разнообразных по составу электродов и электролиту изделий. Только на основе лития работает 12 известных моделей.

В качестве металла электродов могут встретиться:
Принцип действия аккумулятора основан на образовании разности потенциалов между двумя электродами, погруженными электролит. При подключении нагрузки (электротехнических устройств) к клеммам аккумулятора в реакцию вступают электролит и активные элементы электродов. Происходит процесс перемещения электронов, который, по сути, и является электротоком.
Принцип действия аккумуляторов
 Принцип действия аккумулятора основан на образовании разности потенциалов между двумя электродами, погруженными электролит. При подключении нагрузки (электротехнических устройств) к клеммам аккумулятора в реакцию вступают электролит и активные элементы электродов. Происходит процесс перемещения электронов, который, по сути, и является электротоком.
Принцип действия аккумулятора основан на образовании разности потенциалов между двумя электродами, погруженными электролит. При подключении нагрузки (электротехнических устройств) к клеммам аккумулятора в реакцию вступают электролит и активные элементы электродов. Происходит процесс перемещения электронов, который, по сути, и является электротоком.
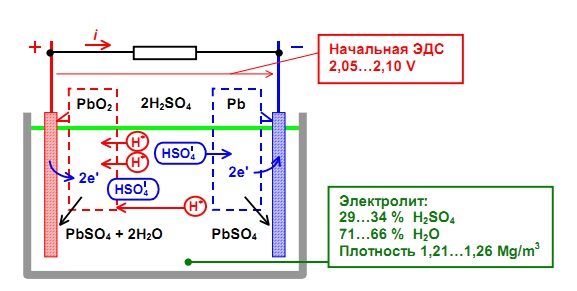
При разряде аккумулятора (подключении нагрузки) губчатый свинец анода выделяет положительные двухвалентные ионы свинца в электролит. Избыточные электроны перемещаются по внешней замкнутой электрической цепи к катоду, где происходит восстановление четырехвалентных ионов свинца до двухвалентных.
При их соединении с отрицательными ионами серного остатка электролита, образуется сульфат свинца на обоих электродах.
Ионы кислорода от диоксида свинца катода и ионы водорода из электролита соединяются, образуя молекулы воды. Поэтому плотность электролита понижается. 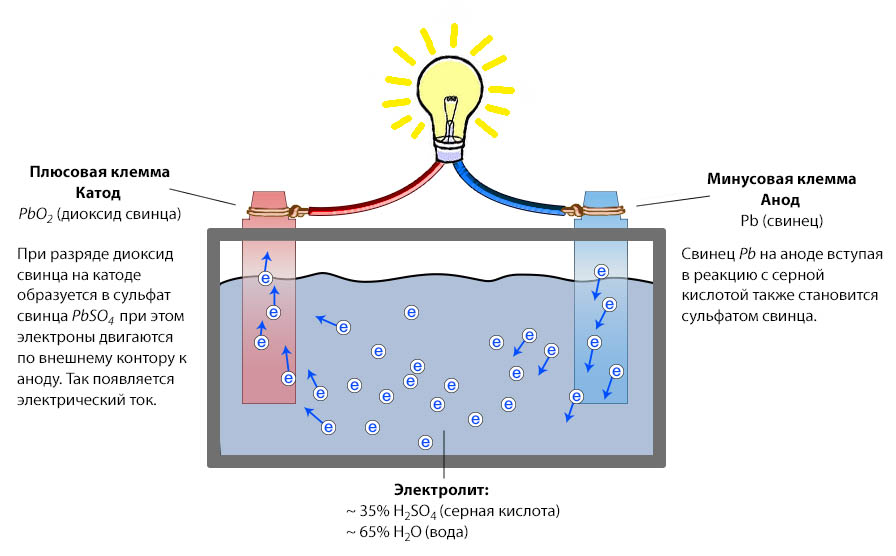
При заряде происходят обратные реакции. Под воздействием внешнего напряжения ионы двухвалентного свинца положительного электрода отдают по два электрона и окисляются в четырехвалентные. Эти электроны движутся к аноду и нейтрализуют ионы двухвалентного свинца, восстанавливая губчатый свинец. На катоде, путем промежуточных реакций, снова образуется двуокись свинца.
Химические реакции в одной ячейке вырабатывают напряжение 2 В, поэтому на клеммах аккумулятора из 6 ячеек и получается 12 В.
Из видео Вы сможете более подробно узнать, как работает аккумулятор:
Аккумуляторные батареи, как и любая другая техника, имеют свое оригинальное устройство, структуру. В современных аккумуляторах используются определенные материалы, внедряются системы, основанные на физических и химических свойствах конкретных веществ и металлов. Рассмотрим принцип работы аккумуляторной батареи на примере свинцово-кислотных.
История аккумуляторов
Первый аккумулятор по официальным данным изобрел в 1798 году Алессандро Вольт – итальянский ученый, разработавший первый химический источник тока.
С 1820 ряд мировых ученых (Ампер, Фарадей, Дэниэл и другие) разрабатывал новые концепции, физические и химические законы, связанные с аккумуляторами.
1899 – Вальдмар Юнгнер разрабатывает батарею, где электродами выступали пластины из кадмия и никеля.
1901 – известный ученый Томас Эдисон изобретает бюджетную по стоимости модель железно-никелевого аккумулятора.
1947 – благодаря ученому Нойману батарея стала полностью герметичной.
1970-е – разработаны первые модели популярных свинцово-кислотных аккумуляторов.
В 1990-х начинается разработка и производство новых моделей аккумуляторов на основе металлгидрида и никеля.
Первый аккумулятор, то есть гальванический элемент многоразового использования, появился, по официальным данным, в 1803 году. Его создал немецкий физик и химик Иоганн Вильгельм Риттер. Друг Эрстеда, Риттер, не будучи ученым, изучал химическое действие света, проводил эксперименты с электролизом, ему, кстати, принадлежит открытие ультрафиолетовой части электромагнитного спектра.
Электрическим аккумулятором называют химический источник тока многоразового действия. Химические процессы внутри аккумулятора, в отличие от оных в одноразовых гальванических элементах, таких как щелочные или солевые батарейки, обратимы. Циклы заряда-разряда, накопления и отдачи электрической энергии, могут многократно повторяться.
Так, сам принцип действия аккумулятора позволяет циклически использовать его для автономного электроснабжения разнообразных устройств, портативных приборов, транспортных средств, медицинского оборудования и т. д. в совершенно различных сферах.

Произнося слово «аккумулятор», имеют ввиду или сам аккумулятор или аккумуляторную ячейку. Несколько последовательно или параллельно соединенных друг с другом аккумуляторных ячеек образуют аккумуляторную батарею, как и несколько соединенных аккумуляторов.
Первый аккумулятор, то есть гальванический элемент многоразового использования, появился, по официальным данным, в 1803 году. Его создал немецкий физик и химик Иоганн Вильгельм Риттер. Друг Эрстеда, Риттер, не будучи ученым, изучал химическое действие света, проводил эксперименты с электролизом, ему, кстати, принадлежит открытие ультрафиолетовой части электромагнитного спектра.
Однажды экспериментируя с вольтовым столбом, Риттер взял пятьдесят кружков из меди, куски влажного сукна, и составил столб из пятидесяти таких кружков и влажного сукна между ними. Пропустив через конструкцию ток от вольтова столба, Риттер обнаружил, что его столб зарядился и сам стал источником электричества. Это и был первый аккумулятор.
Обратимость химической реакции в электролите и на электродах аккумулятора позволяет восстанавливать работоспособность аккумулятора — заряжать его после разряда. Ток в процессе заряда пропускается через аккумулятор в направлении, противоположном разряду.
Так например, свинцово-кислотный аккумулятор работает благодаря электрохимическим реакциям свинца и диоксида свинца в серной кислоте. Формулы ниже отражают обратимые реакции, протекающие на аноде и на катоде: слева направо — реакция при разряде, справа налево — заряд.
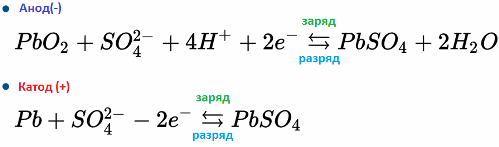
Рассмотрим теперь устройство аккумулятора на примере автомобильной стартерной батареи. Ее напряжение 12 вольт. Состоит батарея из шести соединенных последовательно гальванических элементов, разделенных перегородками.
Последовательное соединение в данном случае обозначает, что отрицательный вывод одной ячейки подключен к положительному выводу следующей ячейки.
Каждый элемент включает в себя пару решетчатых электродов из свинцово-сурьмянистого сплава, погруженных в электролит, представляющий собой 38% водный раствор серной кислоты. Пористый сепаратор изолирует электроды друг от друга, предотвращая замыкания между ними, но свободно пропускает через себя электролит. То есть жидкость заполняет как ячейки свинцовых пластин, так и поры сепараторов.
Одноименные пластины соединены между собой свинцовыми перемычками, как и разделенные перегородками пакеты пластин, составляющие отдельные элементы, и выводы аккумулятора — тоже изготовлены из свинца.
Выводы автомобильного аккумулятора всегда немного отличаются в размере друг от друга — плюсовая клемма больше в диаметре чем минусовая, чтобы не ошибиться при подключении.
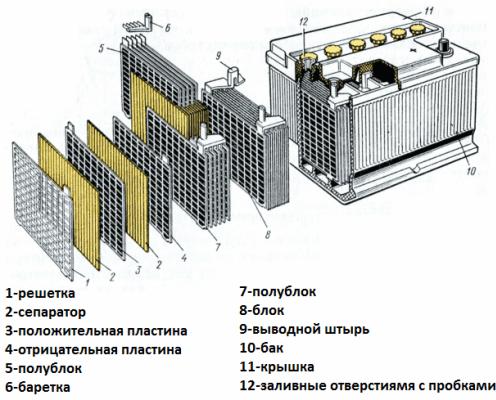
Корпус аккумулятора изготавливается из диэлектрического материала устойчивого к агрессивным средам, к перепадам температур и к вибрациям. Сегодня корпусы стартерных АКБ делают из полипропилена.
Корпус представляет собой герметично закрытую емкость с крышкой, оснащенную отбортовками для прочного крепления. В корпусах старых аккумуляторов всегда предусматривались пробки над каждым из гальванических элементов, составляющих батарею, чтобы можно было при необходимости доливать в них дистиллированную воду. Современные необслуживаемые аккумуляторы пробок на корпусах не имеют.
Другие статьи про аккумумляторы и их использование:
1. Принцип действия
Главная > Доклад >Физика
Принцип действия и использование аккумуляторов
1. Принцип действия
2. Промышленные аккумуляторы
Итальянский ученый Луиджи Гальвани (1737–1798) открыл возможность получения электрического тока иным, чем электризация трением, способом. Однажды, когда он проводил исследование лягушек, он заметил, что при прикосновении стальным скальпелем к нерву лапка мёртвой лягушки пришла в движение. В дальнейшем Гальвани поставил несколько опытов по обнаружению причины возникновения электрического тока
Аккумулятор – прибор для накопления электрической энергии с целью её дальнейшего использования.
1. Принцип действия
Принцип действия аккумуляторов основан на явлении электролиза.
Электролиз заключается в изменение химического состава раствора при прохождении через него электрического тока, обусловленное потерей или присоединением электронов ионами. Важным свойством электролиза является его обратимость
Аналогично гальваническому элементу можно изготовить и аккумулятор. Для этого используют две свинцовые пластины, погруженные в раствор, содержащий одну часть серной кислоты и пять частей воды. Чтобы зарядить аккумулятор, его соединяют последовательно с амперметром и пропускают через цепь ток
Процесс зарядки состоит в том, что две идентичные пластины аккумулятора вследствие электролиза становятся различными; одна из них, отрицательная, по-прежнему остаётся свинцовой, а материал другой (положительной), превращается в перекись свинца
В аккумуляторе протекают следующие химические реакции (в процессе зарядки реакции идут слева направо, при разрядке – в обратном направлении):
4 + 2H 2 O PbO 2 + Pb + H 2 SO 4
2. Промышленные аккумуляторы
Положительные пластины при производстве промышленных аккумуляторов покрывают толстым слоем перекиси свинца. Отрицательные пластины изготавливаются из пористого губчатого свинца
У обычной аккумуляторной батареи, состоящей из трех последовательно соединенных аккумуляторных элементов, напряжение составляет немногим более 6 вольт. Коэффициент полезного действия аккумуляторной батареи – примерно 75%. На аккумуляторной батарее ставят число, которое показывает количество запасенной в аккумуляторе электроэнергии, выраженной в ампер-часах
Например, 120 ампер-часов означает, что при полной разрядке аккумулятор сможет давать ток в 1 ампер в течение 120 часов, или ток в 2 ампера в течение 60 часов
Необходимо постоянно поддерживать аккумулятор в заряженном состоянии. Даже если батарея не находится в эксплуатации, ее следует регулярно подзаряжать. Необходимо содержать зажимы батареи в чистоте и предохранять от возникновения коррозии. Ни следует допускать замерзания батарей
В основном аккумуляторные батареи используются для запуска двигателей автомобилей и других машин. Возможно так же и применение в качестве временных источников электроэнергии в местах, удаленных от населенных пунктов. Необходимо помнить, что аккумуляторы следует поддерживать в заряженном состоянии, применяя для этого, к примеру, солнечную энергию
В будущем аккумуляторы рассчитывают применять для питания экологически чистых электромоторов
1. Кабардин О. Физика: справочные материалы. М.: Просвещение, 1991, 164 с.
2. Трофимова Т.И. Курс физики: Учебное пособие для вузов. М.: Высш. шк., 1999. 542 с.
3. Эллиот Л., Уилкокс У. Физика. М.: ГИФМЛ, 1963, 495 с.
Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: стартерные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Главная > Реферат >Химия
Министерство науки и образования Республики Казахстан
Актюбинский государственный университет им. К. Жубанова
По дисциплине: Физическая химия.
На тему: Аккумуляторы и принцип их работы.
Выполнил: студент Тихонов Тимур
1. Свинцово-кислотный аккумулятор
4. Физические характеристики
5. Эксплуатационные характеристики
7. Свинцово-кислотный аккумулятор при низких температурах
9. Износ свинцово-кислотных аккумуляторов
10. Электри́ческий аккумуля́тор
11. Принцип действия
12. Никель-ка́дмиевый аккумуля́тор
14. Области применения
Свинцово-кислотный аккумулятор — наиболее распространенный на сегодняшний день тип аккумуляторов, изобретен в 1859 году французским физиком Гастоном Планте. Основные области применения: стартерные батареи в автомобильном транспорте, аварийные источники электроэнергии.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в сернокислотной среде. Во время разряда происходит восстановление диоксида свинца на катоде и окисление свинца на аноде. При заряде протекают обратные реакции, к которым в конце заряда добавляется реакция электролиза воды, сопровождающаяся выделением кислорода на положительном электроде и водорода — на отрицательном.
Химическая реакция (слева-направо — разряд, справа-налево — заряд):
В новых версиях свинцовые пластины (решетки) заменяют вспененным карбоном, покрытым тонкой свинцовой пленкой, а жидкий электролит может быть желирован силикагелем до пастообразного состояния. Используя меньшее количество свинца и распределив его по большой площади, батарею удалось сделать не только компактной и легкой, но и значительно более эффективной — помимо большего КПД, она заряжается значительно быстрее традиционных аккумуляторов. [1]
Теоретическая энергоемкость: около 133 Вт·ч/кг.
Удельная энергоемкость (Вт·ч/кг): 30-60 Вт·ч/кг .
Удельная энергоплотность (Вт·ч/дм³): около 1250 Вт·ч/дм³.
ЭДС заряженного аккумулятора = 2,11 В, рабочее напряжение = 2,1 В (6 секций в итоге дают 12,7 В).
Напряжение полностью разряженного аккумулятора = 1,75 — 1,8 В (из расчета на 1 секцию). Ниже разряжать их нельзя.
Рабочая температура: от минус 40 до плюс 40
КПД: порядка 80-90%
Номинальная ёмкость , показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде малым током (1/20 номинальной емкости, выраженной в а/ч).
Стартерный ток (для автомобильных). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев замеряется при -18°С (0°F) в течение 30 секунд. Различные методики замера отличаются, главным образом, допускаемым конечным напряжением.
Резервная емкость (для автомобильных). Характеризует время, в течение которого аккумулятор может отдавать ток 25А. Обычно составляет порядка 100 минут.
Ареометр может быть использован для проверки удельного веса электролита каждой секции
Такие нехитрые операции вместе с проверкой автомобиля на утечку тока и периодической подзарядкой аккумулятора могут на несколько лет продлить срок эксплуатации батареи.
Свинцово-кислотный аккумулятор при низких температурах
Свинцово-кислотные аккумуляторы необходимо хранить только в заряженном состоянии. При температуре ниже −20 °C заряд аккумуляторов должен проводиться постоянным напряжением 2,275 В/секцию, 1 раз в год, в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/секцию в течение 6-12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи и накипи на поверхности аккумулятора создает проводник для тока от одного контакта к другому и приводит к саморазряду аккумулятора, после чего начинается преждевременная сульфатизация пластин и поэтому поверхность аккумулятора необходимо поддерживать в чистоте (то есть его надо мыть перед хранением) Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные (лечебные) циклы, то есть разряд-заряд токами номинальной величины. [2]
Всем этим параметрам и соответствует кислотно-свинцовый аккумулятор, об устройстве которого поговорим ниже.
Обычно для автомобилей применяются кислотно-свинцовые аккумуляторы , которые имеют напряжение 12 вольт и различаются только по емкости заряда. Автомобильный аккумулятор должен обладать несколькими важными параметрами.
- Иметь малое внутренне падение напряжения
- Иметь небольшой саморазряд во время эксплуатации
- Иметь способность выдавать большие токи
- Иметь небольшие габариты и минимальное обслуживание.
Всем этим параметрам и соответствует кислотно-свинцовый аккумулятор, об устройстве которого поговорим ниже.
Элемент Даниэля-Якоби за прошедшие столетия был значительно улучшен и модернизирован. Выработка электричества стала производиться более компактными и производительными устройствами, которые к тому же теперь восстанавливают свой ресурс. Но общий принцип работы аккумулятора остался тот же и сегодня.
Общие сведения
Невозможно представить работу множества современных приборов и механизмов, без аккумулятора – компактного источника жизненной энергии для нашпигованных электроникой и автоматикой всяческих устройств.
Автомобильная стартерная аккумуляторная батарея (АКБ) – так официально называется подобное устройство в транспортных средствах. Хотя принцип работы и конструкцию аккумулятора изучают ещё в средней школе на уроках физики, но многие успевают к началу самостоятельной жизни автолюбителя изрядно забыть столь ценные знания.
Давайте немного оживим наши познания и вспомним, что за штука такая – аккумулятор, как ему удается сохранять и отдавать накопленное электричество. Основной принцип работы аккумулятора – использование эффекта возникновения разности потенциалов (напряжения) между двумя погруженными в раствор электролита металлическими пластинами. Работающий на этом эффекте элемент впервые был сделан в 1836-1838 годах. Одна из пластин в нем была медной, другая цинковой, но она быстро растворялась в электролите.
Элемент Даниэля-Якоби за прошедшие столетия был значительно улучшен и модернизирован. Выработка электричества стала производиться более компактными и производительными устройствами, которые к тому же теперь восстанавливают свой ресурс. Но общий принцип работы аккумулятора остался тот же и сегодня.
Устройство аккумуляторной батареи
Следует уточнить, что французский физик Гастон Плант в 1859 г. создал свинцово-кислотную батарею, площадь которой была всего 10 кв. м. Современный аккумулятор является копией батареи Планта, но только уменьшенной во много раз.
Все детали конструкции батареи объединены в корпусе, который можно видеть как единый элемент аккумулятора под капотом автомобиля.
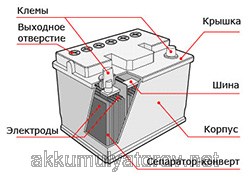
Конечно, правильно было бы называть аккумулятором лишь одну, отдельно взятую ячейку. Несколько таких ячеек должны быть названы аккумуляторной батареей. Так, каждый из шести отдельных аккумуляторов («банок») в стандартной аккумуляторной батарее легкового автомобиля (12 В) вырабатывает напряжение в 2 В.
Крайне серьезные и даже жесткие требования предъявляются к корпусу батареи, который должен обладать достаточной виброустойчивостью, справляться со значительными изменениями температур, а так же выдерживать воздействие агрессивных химических реагентов. Всем этим запросам удовлетворяет современный синтетический материал – полипропилен, именно поэтому в большинстве случаев при изготовлении корпуса используется именно этот материал.

Основная глубокая емкость и закрывающая её крышка – это те части, из которых состоит корпус. Крышка может быть оснащена либо дренажной системой, которая выводит вырабатывающийся газ и стабилизирует давление внутри батареи, либо горловинами с пробками. Вид крышки зависит от типа АКБ.
Каждая из отдельных ячеек аккумуляторной батареи оснащена одним скомбинированным пакетом, который состоит из большого количества пластин с чередованием их полярности. Пластины изготовляются из свинца. Они имеют структуру решеток, состоящих из прямоугольных сот. Именно благодаря такой конструкции можно нанести на пластины активную массу – основной рабочий реагент. Так как данную массу наносят посредством намазывания на пластины, то они так и называются – пластины намазного типа.
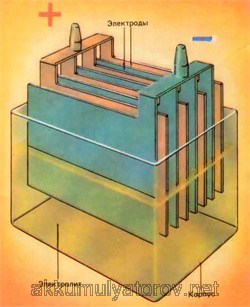
При изготовлении автомобильных аккумуляторов применяются только намазные пластины, хотя существуют и другие типы аккумуляторов. К примеру, в некоторых аккумуляторах устанавливаются пластины с увеличенной площадью, а также пластины из панцирной сетки.
Каждая из пластин в аккумуляторе – это электрод с противоположной полярностью. Именно поэтому может произойти короткое замыкание. Для его предотвращения между каждой парой пластин вставлен, изготовленный из пористого пластика сепаратор, который не препятствует циркуляции электролита внутри ячейки. Чтобы избежать коробления, каждая положительно заряженная пластина помещается между двумя «минусовыми» пластинами. Именно поэтому отрицательных пластин в ячейке всегда на одну больше.
Дабы предотвратить всевозможные деформации и смещения, весь собранный пакет зафиксирован специальным бандажом. При помощи токосборников, плюсовые и минусовые токовыводы пластин концентрируют свою энергию на выводных борнах аккумулятора. К данным борнам подключаются клеммы автомобиля, принимающие ток.
Принцип работы
Двуокись свинца на пластине с положительным зарядом, раствор серной кислоты в воде (электролит, с плотностью 1,28 г/см3), а так же губчатый свинец на отрицательном электроде – это активные элементы, вступающие в реакцию инициирования нагрузки на клеммы аккумулятора. В результате данной реакции происходит процесс вырабатывания электротока, с последующим образованием сульфата свинца на отрицательно заряженной пластине. Так же снижается плотность электролита, так как из него выделяется вода.
К ак известно, аккумуляторы большой емкости больше и массивнее аккумуляторов малой емкости. У них больше рабочая поверхность пластин и больше пространства для диффузии электролита внутри аккумулятора. Поэтому внутреннее сопротивление аккумуляторов большой емкости меньше, чем внутреннее сопротивление аккумуляторов меньшей емкости.
П адение напряжения на свинцовом аккумуляторе не пропорционально разрядному току. При больших разрядных токах, диффузия ионов электролита происходит в свободном пространстве, а при маленьких токах разряда аккумулятора — сильно ограничивается порами активного вещества пластин аккумулятора. Поэтому внутреннее сопротивление аккумулятора при больших токах в несколько раз (для свинцового аккумулятора) меньше, чем внутреннее сопротивление того же аккумулятора при малых токах.
К ак известно, аккумуляторы большой емкости больше и массивнее аккумуляторов малой емкости. У них больше рабочая поверхность пластин и больше пространства для диффузии электролита внутри аккумулятора. Поэтому внутреннее сопротивление аккумуляторов большой емкости меньше, чем внутреннее сопротивление аккумуляторов меньшей емкости.
И змерения внутреннего сопротивления аккумуляторов на постоянном и переменном токе показывают, что внутреннее сопротивление аккумулятора сильно зависит от частоты. Ниже приводится график зависимости проводимости аккумуляторов от частоты, который взят из работы австралийских исследователей.
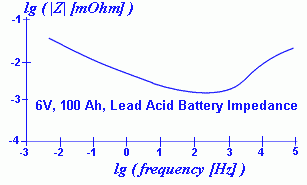
И з графика следует, что внутреннее сопротивление свинцового аккумулятора имеет минимум при частотах порядка сотен герц.
П ри высокой температуре скорость диффузии ионов электролита выше, чем при низкой. Эта зависимость имеет линейный характер. Она и определяет зависимость внутреннего сопротивления аккумулятора от температуры. При более высокой температуре, внутреннее сопротивление аккумулятора ниже, чем при низкой температуре.
В о время разряда аккумулятора, количество активной массы на пластинах аккумулятора уменьшается, что приводит к уменьшению активной поверхности пластин. Поэтому внутреннее сопротивление заряженного аккумулятора меньше, чем внутреннее сопротивление разряженного аккумулятора.
Отправить заявку
Аккумуляторы по новым технологиям
При всех этих конструктивных отличиях общий принцип работы и протекания электрохимических процессов внутри батарей остается прежним.
Но, к сожалению, все эти разработки крайне медленно приближаются к коммерческому уровню поскольку все они пока не вышли в массовое производство, не доказали свои практические преимущества, а пробные партии имеют несравнимо высокую цену по сравнению с традиционными, проверенными временем, выпускаемых серийно промышленных образцов аккумуляторных батарей.
- Чем больше объем двигателя, тем более емкий аккумулятор требуется;
- В дизельных моторах используются АКБ с большей емкостью, чем в бензиновых, того же объема;
- Если вы эксплуатируется автомобиль в условиях сильных морозов, нельзя покупать гелиевые АКБ.
Приобретая аккумулятор для своего автомобиля, не обязательно знать все параметры и характеристики, указываемые на батарее, а только к какой категории принадлежит ваш ДВС и какой объем двигателя у вашего автомобиля. Из особенностей которые нужно учитывать при выборе АКБ можно выделить следующее:
- Чем больше объем двигателя, тем более емкий аккумулятор требуется;
- В дизельных моторах используются АКБ с большей емкостью, чем в бензиновых, того же объема;
- Если вы эксплуатируется автомобиль в условиях сильных морозов, нельзя покупать гелиевые АКБ.
Конечно многие обращают внимание и на другие параметры, указанные на аккумуляторе, что не обязательно. Обычно на самой батарее или в ее названии указывают какого типа батарея (например стартерная), ее емкость, мощность, время заряда, масса залитой батареи, параметры согласно стандартов других стран.
Перед тем как покупать АКБ, изучите технический паспорт своего транспортного средства, либо ознакомьтесь с параметрами старой батареи – это поможет не ошибиться с выбором и правильно сделать выбор с учетом особенностей вашего автомобиля. Если самостоятельно выбрать аккумулятор не получается, можно обратиться за консультацией к специалисту, например, к продавцу в автомобильном магазине.
http://pue8.ru/elektricheskie-seti/805-kak-rabotaet-akkumulyator-i-iz-chego-on-sostoit.html
http://kwatt.com.ua/chto-takoe-akkumulyator-osnovnye-ponyatiya-printsip-raboty-i-nemnogo-istorii/
http://electrik.info/device/1297-ustroystvo-i-princip-raboty-akkumulyatora.html
http://works.doklad.ru/view/1VR7KGsSkvI.html
http://works.doklad.ru/view/CDmtTwVmOa0.html
http://autoustroistvo.ru/elektrooborudovanie/akb/
http://akkumulyatorov.net/ustrojstvo-i-princip-raboty-akkumulyatora/
http://www.at-systems.ru/quest/new-quest/battery-resistance-y.shtml
http://wybor-battery.com/stati/tendencii-razvitiya-akkumulyatornyh-batarej/
http://vtorbaza.com/spravka/iz-chego-sostoit-avtomobilnyj-akkumulyator/